
Foto: Matt Wilson/Jay Clark, NOAA NMFS AFSC
Fakta
Havforsuring
Havet tar opp omtrent en fjerdedel av all CO2 menneskene slipper ut i atmosfæren. Uten dette ville temperaturen allerede ha steget mer enn to grader siden førindustriell tid. Prisen vi betaler er at CO2-opptak gjør vannet surere, til skade for økosystemene i havet. Hvis CO2-utslippene fortsetter som nå, kan havforsuring ha en betydelig påvirkning på marine økosystem.
Oppdatert 30. mars 2026
Hvert år slipper vi ut omtrent 40 gigatonn (Gt) karbondioksid (CO2) i atmosfæren, ved forbrenning av fossile brennstoff og endringer i arealbruk. Dette er kjent som antropogent eller menneskeskapt CO2. Omtrent en fjerdedel eller 10 Gt CO2 blir tatt opp i havet. I tiden etter den industrielle revolusjon har havet absorbert CO2 tilsvarende 26 prosent av våre samlede utslipp.
På denne måten har havet gjort oss en tjeneste og dempet klimaendringene. Om ikke havet hadde tatt opp antropogent CO2, ville nivået av CO2 i atmosfæren nå vært 500 ppm (milliondeler), og den globale gjennomsnittstemperaturen ville ha økt mer enn to grader siden førindustriell tid. Da ville vi allerede ha vært langt over togradersmålet, som verdens land i Paris-avtalen ble enige om at representerer en grense for «akseptabel klimaendring».

Figur 1. Havet og atmosfæren utveksler alltid CO2. Så lenge det er likevekt, transporteres det like mye begge veier (venstre bilde). Når CO2-konsentrasjonen i atmosfæren øker (midtbildet), forstyrres balansen, og mer CO2 overføres til havet – til ny likevekt eventuelt er oppnådd (høyre bilde). Illustrasjon: Ellen Viste
Havets tjenester kommer likevel med en kostnad. Når CO2-konsentrasjonen i havet stiger, skjer det en kjemisk reaksjon som reduserer vannets pH og gjør vannet surere. Dette er kjent som havforsuring og vil sannsynligvis ha alvorlige konsekvenser for de marine økosystemene.
Hvorfor er dette viktig?
Havforsuring er et globalt problem som kan ha alvorlige konsekvenser for marine organismer og økosystemer. Hvis vi fortsetter å slippe ut CO2 i samme hastighet som nå, vil havforsuringen sannsynligvis føre til tap av biodiversitet og en reduksjon i ressurser som kan høstes, inkludert dem vi tenker på som mat for mennesker. Den eneste måten å stoppe havforsuring på er å redusere utslippene av CO2.
Hva er havforsuring?
Havvannet inneholder karbonat (CO32-). Disse ionene kan reagere kjemisk med CO2.

Figur 2. I vannet reagerer CO2 med vannmolekyler og karbonat (CO32-) og danner bikarbonat (også kjent som hydrogenkarbonat HCO3-). Dermed blir det mindre CO2 i overflatevannet, som kan fortsette å ta opp CO2 fra atmosfæren. Illustrasjon: Ellen Viste
Du finner flere detaljer om den kjemiske reaksjonen her (PDF).
Omtrent 95 prosent av all antropogent CO2 som tas opp i havet reagerer med oppløste karbonationer i vannet. Derfor minker nå konsentrasjonen av karbonat i havet, mens konsentrasjonen av bikarbonat øker. Siden bikarbonat er surere enn karbonat, gjør dette havet surere og pH-verdien synker.
De resterende 5 prosentene CO2 som ikke løses opp i vannet er en syre, og det senker pH-verdien enda mer. Derfor blir havet surere jo mer CO2 det tar opp fra atmosfæren. Dette er havforsuringens natur.
Hva er pH?
Enheten pH er et mål for hvor surt noe er. Skalaen regnes normalt fra 0 til 14, men høyere og lavere verdier kan forekomme. Rent praktisk definerer den konsentrasjonen av hydrogenioner [H+] i en væske.
En væske med pH-verdi på sju vil være nøytral. Syrer har pH under sju og baser høyere enn sju.

Figur 3. pH beskriver vannets surhet. En væske med pH-verdi lik 7 er nøytral. Høyere verdier betyr at væsken er basisk; lavere pH at den er sur. Sjøvann har normalt pH-verdi på litt over 8 og er derfor svakt basiskt. Pdf-versjon finner du her. Illustrasjon: Ellen Viste
Hva har forskerne funnet?
Observasjoner av havets karbonopptak og forsuring
De siste tiårene har forskere verden over gjort systematiske målinger av de kjemiske forholdene i havet. Dataene viser klart at CO2-nivåene har steget og pH-verdiene sunket. CO2-konsentrasjonen i havoverflaten stiger like raskt som i atmosfæren, og pH-verdien følger etter.
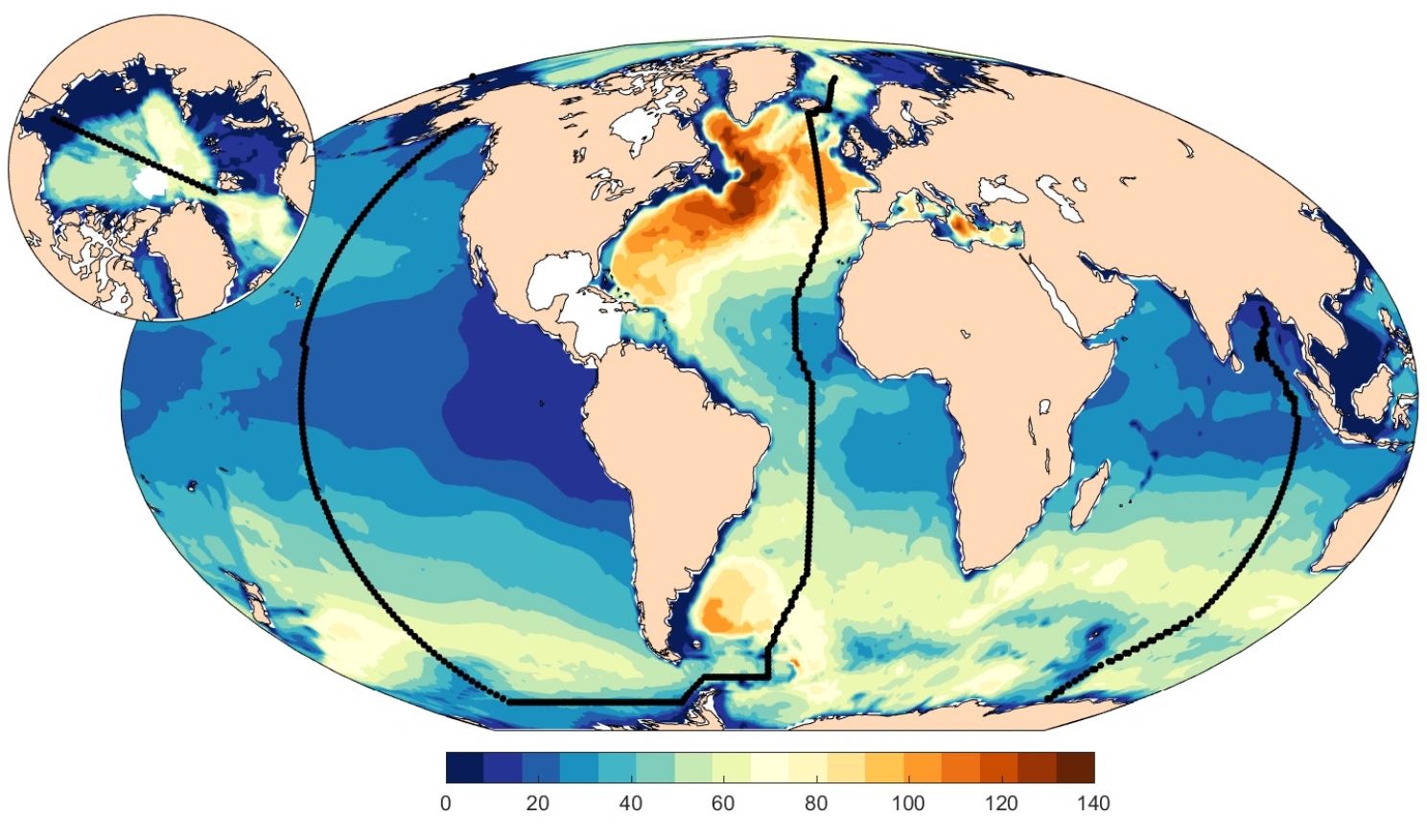
Figur 4. Fordeling av antropogent CO2 i havet [mol C m-2]. Brunt representerer høye verdier, blått lave. Den svarte kurven viser hvor tverrsnittet i figur 5 er tatt. Ill.: Siv K. Lauvset, med data fra GLODAPv2, publisert i Lauvset et al. (2016). Ill.: Nadine Goris
Mellom 1800 og 2016 har pH-verdien i overflatevannet sunket fra 8,2 til 8,1 i gjennomsnitt. Det høres ikke mye ut, men fordi pH-skalaen er logaritmisk, tilsvarer det en økning i surhet på 25 prosent.
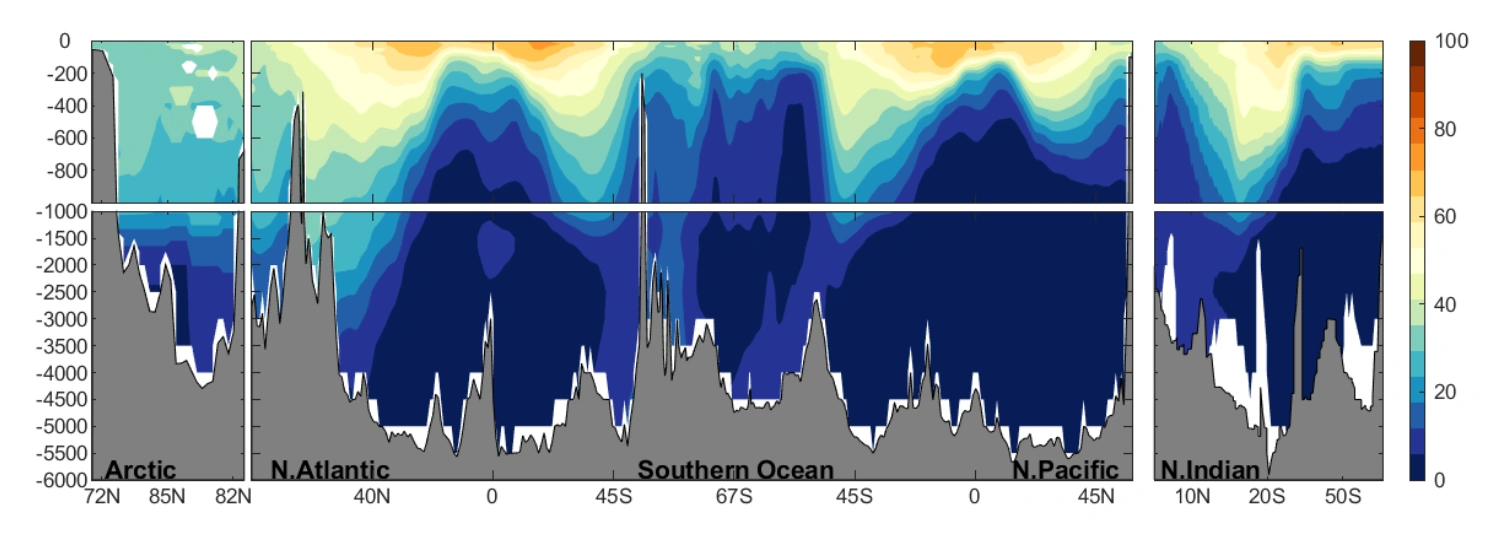
Figur 5. Fordeling av antropogent CO2 i et tverrsnitt gjennom Atlanterhavet, Sørishavet og Stillehavet. Data og kilde som i figur 4. Ill.: Siv Kari Lauvset
Verken antropogent CO2 eller havforsuring er jevnt fordelt i havet. Mest antropogent CO2 finnes i Nord-Atlanteren og Sørishavet. I disse områdene synker tungt overflatevann, og CO2 transporteres fra overflaten og helt til bunns. Nedsynkningen er med på å frakte vann rundt i verdenshavene og blir ofte sammenlignet med ettransportbånd - havets transportbånd.
Antropogent CO2 som har fulgt det synkende vannet nedover i dypet, transporteres videre gjennom verdenshavene og kan til slutt påvirke alle deler av verden. Dette er med på å drive havets CO2-opptak.

Figur 6. Både havstrømmer og biologi fører til at karbon fraktes nedover i havet. Kaldere vann kan ta opp mer CO2 fra atmosfæren. I noen havområder, som i Nord-Atlanteren, blir overflatevannet avkjølt og synker (venstre bilde). Dermed fraktes vann mettet med CO2 nedover i dypet, mens overflatevannet som strømmer inn kan fortsette å få overført CO2 fra atmosfæren. De nordiske hav er et av områdene der dette skjer. Planteplankton omdanner CO2 til organisk materiale gjennom fotosyntese. Når plankton – eller dyr som har spist dem – dør, synker de (høyre bilde). Dermed fraktes organisk karbon nedover i dypet. Der bryter bakterier ned det organiske materialet til CO2, som spres med havstrømmene gjennom verdenshavene. Det kan ta tusener av år før denne CO2-en igjen når overflaten. Pdf-versjon finner du her. Illustrasjon: Ellen Viste
Fremtiden
Jordsystemmodeller er matematiske modeller som inneholder både det fysiske klimasystemet og kjemiske og biologiske kretsløp. Disse modellene beregner fremtidens klima og havets CO2-opptak basert på ulike tenkte utviklinger av menneskelig CO2 -utslipp.
Forskningsinstitutt og universiteter verden over driver flere jordsystemmodeller. Alle modellene viser at havets opptak av CO2 og havforsuring først og fremst vil avgjøres av hvor mye CO2 menneskene slipper ut i atmosfæren. Derfor er det helt nødvendig å redusere CO2-utslippene for å unngå at havet blir enda surere.
Jordsystemmodellene viser også at Sørishavet og Nord-Atlanteren vil fortsette å ta opp CO2 fra atmosfæren. I begge regionene vil opptaket avhenge av havsirkulasjonen og den biologiske produksjonen. Alle modellene viser at klimaendringer vil redusere havets opptak av CO2 noe. Det vil føre til at en større andel av den CO2-mengden vi slipper ut vil forbli i atmosfæren. Dermed forsterkes klimaendringa.
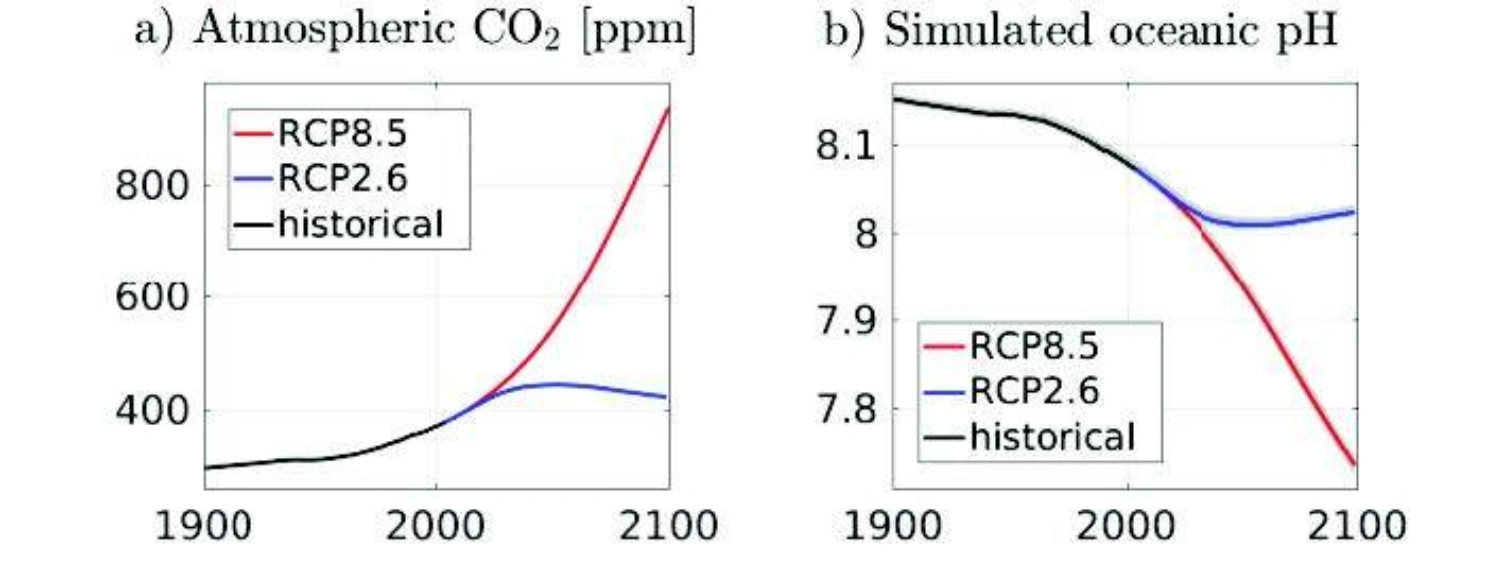
Figur 7. a) Konsentrasjon av CO2 i atmosfæren hvis CO2-utslippene ikke reduseres i fremtiden (RCP8.5, rødt) og hvis de reduserer sterkt (RCP2.6). b) Endring i global pH-verdi i havet ved ingen (RCP8.5, rød) og sterk (RCP2.6, blå) reduksjon i CO2-utslipp. Åtte jordsystemmodeller er brukt i simuleringen. RCP - Representative Concentration Pathway - viser til en tenkt utvikling av CO2-utslipp.
Havforsuring påvirker økosystemer
Flere arter har vist seg å ta skade av havforsuring. Eksempler på dette er koraller, vingesnegl (pteropoder) og muslinger. Både korallrev og skjell er laget av mineraler som inneholder karbonat. Siden konsentrasjonen av oppløste karbonationer er lavere når vannet er surere, vil det bli vanskeligere for disse organismene å få tilgang til mineralene de trenger.
Når vannet blir undermettet på karbonat, vil det være utfordrende for slike organismer å overleve. Hvis CO2-utslippene fortsetter å øke med dagens hastighet, viser jordsystemmodellene at havforsuring vil føre til undermetning av karbonat i Arktis og Sørishavet innen utgangen av dette århundret. Dette kan ha skadelige virkninger på vingesnegl og kaldtvannskoraller i disse områdene, fordi skallene og rev-strukturene er laget av karbonat.
En studie av Guinotte og kolleger publisert i 2003 viste at områder der rev av varmtvannskoraller lever er blitt redusert fra 1800 til 2002 på grunn av havforsuring som skyldes havets CO2-opptak. Jordsystemmodeller viser at dersom CO2-utslippene fortsetter med uforminsket styrke (RCP 8.5), vil alle leveområdene for varmtvannskoraller være tapt innen år 2100.
Noen studier viser at også høyere nivåer i næringskjeden kan bli påvirket. For eksempel reagerer noen fiskearter i mindre grad på truende predatorer fordi havforsuring kan påvirke nevrologiske prosesser i fisk. Andre fiskearter viser ingen slik respons. Mange voksne fisker har sannsynligvis høy toleranse for havforsuring i seg selv, men effektene på plankton og korallrev kan påvirke fiskens mattilgang eller habitat negativt.
Havforsuring i kombinasjon med andre stressfaktorer vil virke inn på de marine økosystemene. Klimaendring fører til varmere hav og lavere oksygeninnhold. Et varmere hav vil være mer lagdelt og stabilt, slik at dypere vann i mindre grad blandes opp. Derfor venter man lavere nivåer av næringsstoffer i de øvre vannmassene. Dette vil forverre effektene av havforsuring. For eksempel vil det å opprettholde karbonatskall kreve mer energi når vannet er surere, og med mindre næringsstoffer vil denne energien vil være vanskeligere tilgjengelig.
Å bestemme den samlede effekten av slike stressfaktorer på marine økosystem er en av våre store vitenskapelige utfordringer. Det er vanskelig å utforme gode eksprimenter og å drive med over lang tid. I tillegg er marine økosystemer og marine organismer av natur svært forskjellige, og siden de fleste studiene til nå har vært utført på en enkel art eller underart, er det usikkert hvordan hele økosystemer vil reagere på havforsuring.
Den totale effekten av sammensatte stressfaktorer vet vi enda mindre om. Til tross for dette ventes havforsuring å ha store og mest sannsynlig negative konsekvenser for økosystemene.
Marine matressurser og havforsuring
Områder med høy marin produksjon er ofte hovedkilde til proteinrik mat i kystsamfunn. Jordsystemmoldeller tyder på at mange av disse områdene er svært sårbare for havforsuring i dette århundret. Fordi verdens befolkning øker, er det sannsynlig at også behovet for mat fra havet vil øke. Havforsuring utgjør en ny trussel for fiskestammer som i mange områder allerede er truet av overfiske og klimaendringer.
Innen akvakultur er marine virvelløse dyr, som muslinger, hummer og reker, mest sårbare for havforsuring, fordi denne kan hemme veksten av skall og fysiologi. Fiskeri og akvakultur er av stor betydning for nåværende og fremtidig matsikkerhet. Disse industriene er risikoutsatte, fordi havforsuring påvirker organismene både direkte og indirekte gjennom næringskjeden og habitatene de er avhengige av.
Havforsuring ved Norskekysten
Havforsuring i norske farvann er målt siden 1990-tallet, og overvåkning i statlig regi startet i 2013.
Å dokumentere trender i forsuring av kyst- og fjordvann er vanskeligere enn ute i det åpne havet. Forholdene varierer både fra sted til sted og over tid. Data fra fjordene sør for Bergen viser at pH-verdien kan variere like mye gjennom et døgn som den kan gjøre fra måned til måned eller fra år til år.
Vingesneglen i Norskehavet og Barentshavet vil være spesielt utsatt for havforsuring. Dypvannskorallrevene langs store deler av Norskekysten er også i faresonen.
Hva er blitt gjort?
Den eneste måten å stoppe havforsuring på er å begrense utslippene av CO2 til atmosfæren, fordi CO2 som slippes ut i atmosfæren etter hvert vil havne i havet. De siste årene har det blitt satt i gang mange aktiviteter for å redusere CO2-utslippene. Den viktigste er Paris-avtalen fra 2015. Der forpliktet verdens land seg til å redusere utslippene slik at global oppvarming ikke ville overstige to grader.
Det er etablert flere nettverk for å overvåke og tallfeste havets opptak av CO2 og havforsuring. Noen eksempler på dette er Global Ocean Acidification Observation Network med sine regionale nettverk, Ocean Acidification International Reference User Group of the European Project on Ocean Acidification, og International Alliance to Combat Ocean Acidification. Et annet viktig nettverk er Integrated Carbon Observation System. Dette er en europeisk infrastruktur som overvåker og kvantifiserer karbonflukser fra atmosfæren, havet og landjorden.
Internasjonale datasett som GLODAP og SOCAT er kvalitetskontrollerte karbonmålinger som er samlet inn av forskerne verden over og gjort tilgjengelig for alle.
Hva må vi gjøre?
Selv om vi skulle slutte å slippe ut CO2, vil ikke havet være i fullgod stand igjen med en gang. Den CO2 vi har sluppet ut i atmosfæren de siste 200 årene finnes der fremdeles og vil bli tatt opp havet i årene fremover. Havforsuring nøytraliseres bare ved at vulkanske bergarter forvitres og ved at sedimenter frigjør karbonationer til havet. Dette er prosesser som går veldig sakte, og det vil ta tusener av år før havet vil bli mindre surt igjen. Likevel er det å redusere utslipp av CO2 til atmosfæren den meste effektive måten å stoppe havforsuring på.
Det er blitt foreslått tiltak som kan dempe temperaturstigningen selv omCO2-konsentrasjonen i atmosfæren øker. Slike tiltak vil ikke forhindre havforsuring. Så lenge CO2-konsentrasjonen i atmosfæren stiger, vil også havet ta opp mer CO2 og bli surere.
På samme tid er havforsuring bare én av flere stressfaktorer for økosystemene i havet. Andre faktorer er oppvarming, reduksjon av oksygen, tap av næringsstoffer i de øverste vannmassene, fiske og plastforurensning. På liten skala kan det hjelpe å redusere CO2-innhold og havforsuring ved å plante tang, sjøgress og andre alger. Men det vil bli vanskelig å opprettholde dette over lengre tid.
Å redusere CO2-utslippene vil ikke bare redusere havforsuringen globalt, men også redusere oppvarmingen og mange av de andre stressfaktorene. Koraller er spesielt sårbare overfor stigende temperatur. Episoder med korallbleking i de senere årene er et resultat av høy sjøtemperatur.
De biologiske konsekvensene av havforsuring er usikre, men mest sannsynlig negative, særlig i kombinasjon med andre stressfaktorer. For å sikre en sunn planet, bør vi følge føre var-prinsippet og stoppe utslipp av CO2 til atmosfæren nå.
Referanser
Bakker et al. (2016). A multi-decade record of high quality fCO2 data in version 3 of the Surface Ocean CO2 Atlas (SOCAT, Earth Syst. Sci., Data, 8, 383-413
Friedlingstein et. al. (2023). Global Carbon Budget 2023, Earth Syst. Sci. Data, 15, 5301-5369
Guinotte, J. M., Buddemeier, R. W., & Kleypas, J. A. (2003). Future coral reef habitat marginality: temporal and spatial effects of climate change in the Pacific basin. Coral Reefs, 22(4), 551-558
Goris et al. (2018) Constraining Projection-Based Estimates of the Future North Atlantic Carbon Uptake. J. Climate, 31, 3959–3978
Jones et al. (2022). Monitoring ocean acidification in Norwegian seas in 2021, Report, Norwegian Environment Agency, M-2311, 2022
Kontaktpersoner

Are Olsen
Professor - Research leader, Carbon System, UiB - Universitetet i Bergen

Siv Kari Lauvset
Forsker II / Researcher II - Carbon System, NORCE

Nadine Goris
Forsker II / Researcher II - Co-leader, Carbon System, NORCE

Ingunn Skjelvan
Forsker II / Researcher II - Carbon System, NORCE